NOVAMag® membrane
MEMBRANA REABSORBIBLE DE MAGNESIO

Membrana de barrera reabsorbible
Metal biodegradable
Degradación controlada
La membrana de magnesio es mecánicamente fuerte y reabsorbible al mismo tiempo. Puede recortarse a medida y moldearse para tratar defectos óseos individuales. Dado que NOVAMag® membrane se reabsorbe completamente a los pocos meses de su implantación, no es necesaria una segunda intervención quirúrgica para retirar la membrana.
Mecánicamente fuerte y reabsorbible
NOVAMag® membrane se fabrica a partir de magnesio metálico puro. El magnesio es un metal biodegradable que el cuerpo humano reabsorbe sin dejar residuos tóxicos1-3. Los iones de magnesio (Mg2+) liberados durante el proceso de degradación son un componente natural del cuerpo humano y son responsables de muchos procesos fisiológicos4-6. Debido a las propiedades inherentes del magnesio metálico, NOVAMag® membrane proporciona una opción de material mecánicamente resistente pero degradable para las cirugías de aumento óseo7-8. Es ideal para proteger los huecos de los defectos óseos durante la regeneración ósea y mantener la posición del hueso autólogo y los materiales de aumento óseo como cerabone®.
Estás viendo un contenido de marcador de posición de Vimeo. Para acceder al contenido real, haz clic en el siguiente botón. Ten en cuenta que al hacerlo compartirás datos con terceros proveedores.
Más información- en caso de defectos óseos quirúrgicos y defectos de la pared ósea
- en el contexto del aumento del suelo sinusal
- en el contexto del aumento de el reborde alveolar
- en el contexto de la reconstrucción de crestas para el tratamiento protésico
- en el contexto de un tratamiento de defectos de fenestración
- en caso de defectos óseos periodontales (defectos de una a tres paredes, defectos de furcación)
- tras apicectomía, cistectomía, resección de dientes retenidos y resección de otras lesiones óseas
- en alveolos de extracción tras extracciones dentales
- en caso de GBR junto con la colocación inmediata o diferida del implante
- Considerar la gestión de los tejidos blandos
- No dejar bordes afilados en la membrana
- 3 – 4 mm de solapamiento de la membrana sobre las paredes del defecto
- Suavizar el borde de la membrana con el moldeador NOVAMag® sculptor
- Doblar la membrana para darle forma utilizando el moldeador NOVAMag® sculptor, eliminando las fuerzas restauradoras
- Dar forma a la membrana antes de colocarla
- La membrana se puede fijar con tornillos NOVAMag® fixation screw XS o tornillos de titanio
- Fijar la membrana tanto en el lado bucal como en el lado palatino-lingual
Origen: Sintético
Composición: Magnesio (Mg)
Espesor: 140 ± 20 μm
Fijación: En un tratamiento GBR, la membrana debe inmovilizarse completamente a ambos lados del defecto (oral y bucalmente) con NOVAMag® fixation screw XS u otros sistemas de fijación disponibles en el mercado compuestos por tornillos de titanio.
Tiempo de degradación: Reabsorbible (en 2-4 meses)
- Metal biodegradable
- Sintético
- Membrana de barrera reabsorbible
- Degradación controlada (es decir, sin desintegración precoz, sin encapsulación).
- No es necesaria la cirugía de extirpación, lo que supone menos intervenciones quirúrgicas y menos tiempo de sillón
Distribución
Con nuestra red internacional de socios de distribución, estamos cerca de usted en más de 100 países en todo el mundo. Además de nuestro portafolio de productos 360°, ofrecemos servicio, asesoramiento científico e intercambio, formación y eventos directamente en el lugar, todo desde una sola fuente.
Encuentre un socio de distribución cerca de usted:
PREGUNTAS FRECUENTES
PRODUCTOS RELACIONADOS

NOVAMag® fixation screw
Aleación metálica de magnesio reabsorbible y biodegradable
Ideal para fijar membranas de barrera, injertos óseos y material de aumento óseo
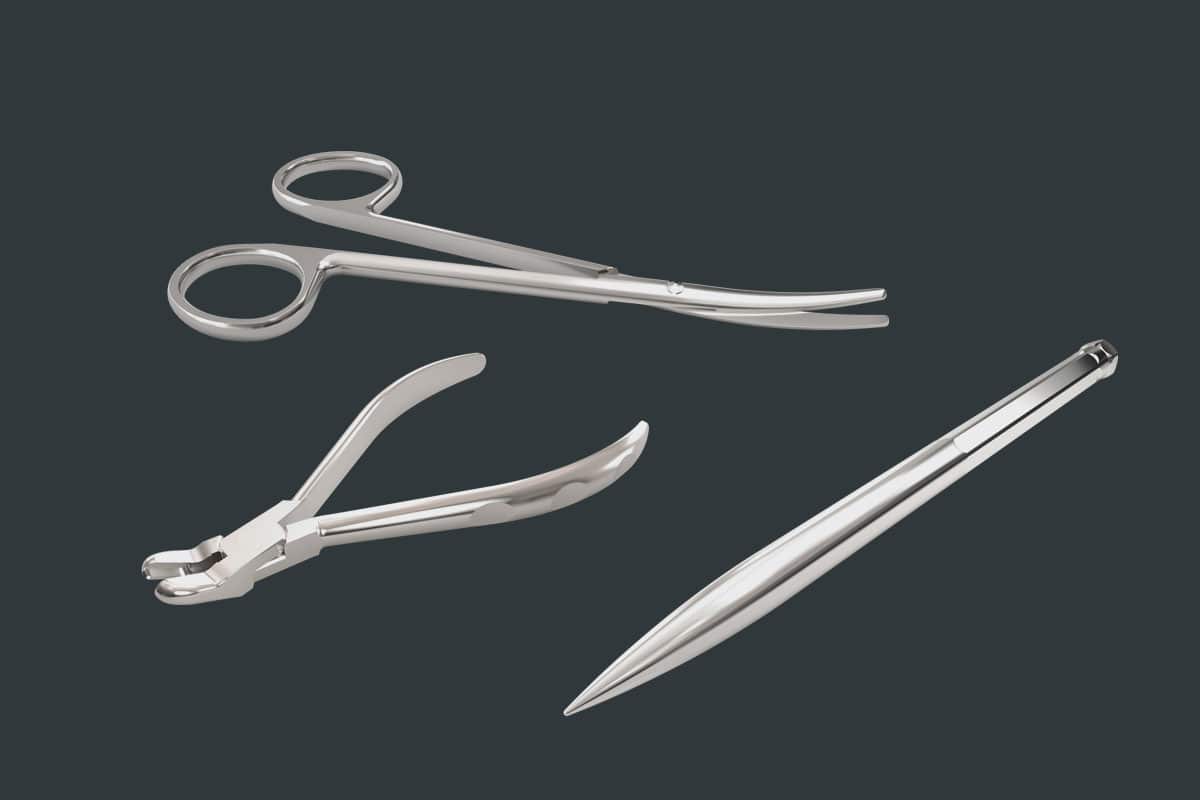
NOVAMag® Instruments
Manipulación óptima de todos los productos de magnesio
Para garantizar una manipulación óptima de la membrana NOVAMag® y del tornillo de fijación NOVAMag®, botiss ha desarrollado una gama de instrumentos NOVAMag® en estrecha colaboración con los clínicos.

permamem®
MEMBRANA DE BARRERA DE PTFE DE ALTA DENSIDAD
Una membrana excepcionalmente fina, no reabsorbible y biocompatible.