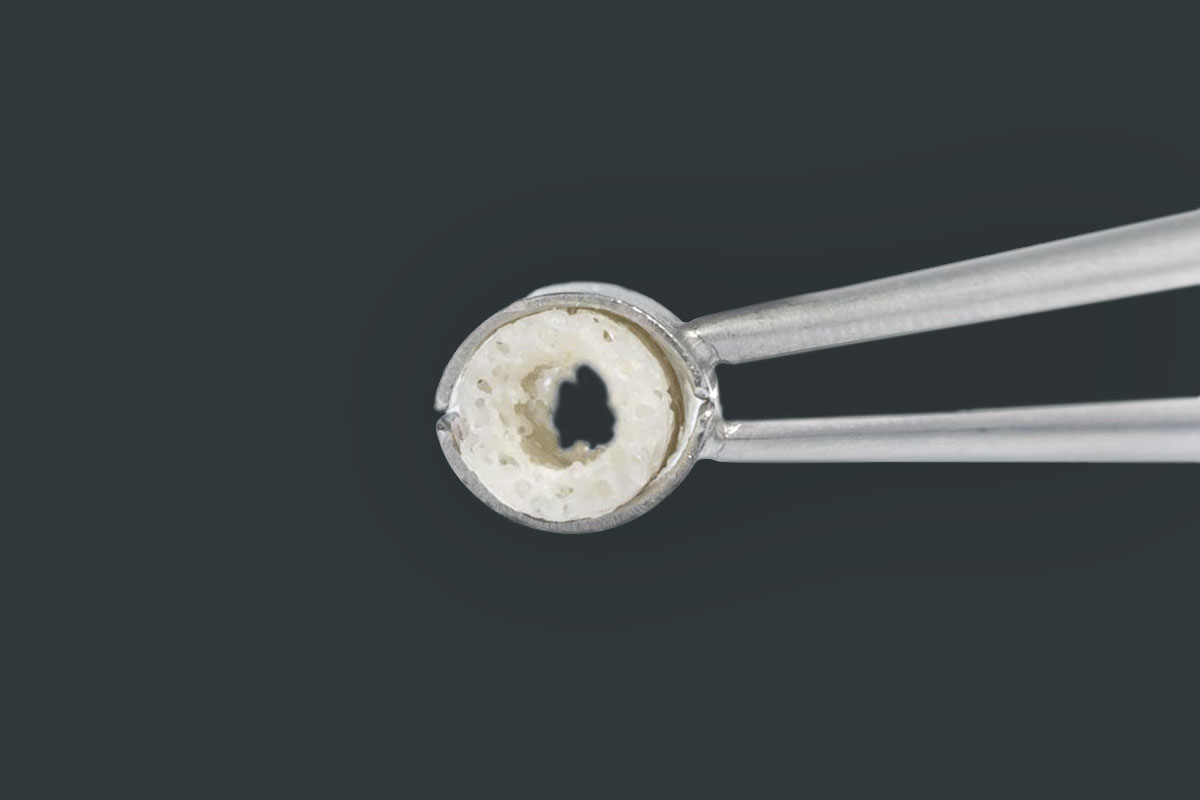
maxgraft® bonering
AUGMENTATION OSSEUSE ET POSE D'IMPLANTS SIMULTANÉES

confort DU patient
TEMPS DE TRAITEMENT PLUS COURTS
Procédure en une étape
maxgraft® bonering est un anneau spongieux préfabriqué à partir d’os de donneurs humains traité. maxgraft® bonering permet la mise en place de l’implant et l’augmentation osseuse en une seule étape1.
RECONSTRUCTION RAPIDE DE L’OS
Avec la technique de l’anneau osseux, la durée du traitement peut être raccourcie de plusieurs mois, car une deuxième opération pour la pose de l’implant est évitée. L’intégration osseuse de l’anneau osseux et de l’implant se fait sur l’os vital environnant. Après une période de cicatrisation de six mois, la réouverture et la restauration prothétique peuvent avoir lieu. L’utilisation d’un anneau osseux allogène au lieu de l’os du patient peut améliorer le confort du patient. Les risques associés au prélèvement d’os autogène, tels que la morbidité du site donneur, le risque accru d’infection et la douleur postopératoire, peuvent être évités ou prévenus1,2.
ACCEPTATION ÉLEVÉE PAR LES PATIENTS – TEMPS DE TRAITEMENT PLUS COURTS
Grâce à sa grande capacité de régénération biologique et à son remodelage complet, maxgraft® représente une alternative à l’os du patient. La nécessité d’un deuxième site chirurgical est éliminée, la durée de l’opération est raccourcie et la douleur et la morbidité postopératoires pour le patient sont considérablement réduites.
IMPLANTOLOGIE, CHIRURGIE ORALE ET CMF
- Augmentation verticale (défauts tridimensionnels avec augmentation horizontale de faible ampleur)
- Espace entre deux dents
- Espace édenté
- Élévation du plancher sinusien (hauteur osseuse résiduelle de 4 mm à 1 mm)
Contre-indications :
- Crête alvéolaire très étroite à parois parallèles
- Hauteur osseuse résiduelle inférieure à 1 mm dans le sinus
Réhydratation
Le processus de production de maxgraft® préserve le collagène naturel et une humidité résiduelle de <10%. Il est néanmoins recommandé de réhydrater maxgraft® bonering avant utilisation (10 min dans une solution saline). La réhydratation dans une solution saline améliore la flexibilité de l’anneau (en particulier pour l’anneau de 7 mm), ce qui le rend moins susceptible de se fracturer et permet de l’adapter plus facilement à la zone défectueuse.
Préparation du site d’implantation avec le maxgraft® bonering surgical kit
Avec le maxgraft® bonering surgical kit tous les instruments nécessaires à l’application de la technique de l’anneau osseux sont fournis. Pour des informations plus détaillées sur la procédure chirurgicale, veuillez vous référer au guide chirurgical de maxgraft® bonering.
En combinaison avec cerabone®
L’utilisation simultanée de maxgraft® bonering et de cerabone® combine les avantages des substituts osseux allogènes et bovins – le potentiel biologique de maxgraft® et la stabilité volumique de cerabone®, qui protège contre la résorption et améliore le résultat esthétique.
Régénération osseuse guidée – Utilisation d’une membrane barrière
maxgraft® bonering doit être recouvert d’une membrane ayant une fonction de barrière suffisamment longue (par exemple la membrane Jason® ) pour obtenir une régénération osseuse contrôlée et empêcher la prolifération des tissus mous.
Fermeture de la plaie
Il est nécessaire de tenir compte de la situation des tissus mous avant l’intervention chirurgicale. La plaie doit être fermée sans tension. La mobilisation en chevauchement des tissus mous avant la suture doit être possible.
Réinsertion
maxgraft® bonering est fixé sur l’os avec une stabilité primaire à l’aide d’un implant approprié. La restauration prothétique de l’implant doit avoir lieu environ 6 mois après l’implantation pour éviter la résorption due à une charge mécanique insuffisante. Le moment approprié pour la mise à nu de l’implant est déterminé individuellement par le praticien.
- Procédure en une étape : augmentation osseuse et pose d’implants simultanées
- Anneau d’os spongieux, disponible en différentes tailles (en fonction de l’implant)
- Concept de traitement innovant
- Propriétés ostéoconductrices qui favorisent un remodelage naturel et contrôlé

Spécifications DU produit
maxgraft® bonering 3.3
Recommandé pour des implants de diamètres de 3,3 à 3,5 mm
| N° d’art. | Dimension | Contenu |
|---|---|---|
| 33160 | anneau spongieux, ø 6 mm, hauteur 10 mm
|
1 x |
| 33170 | anneau spongieux, ø 7 mm, hauteur 10 mm
|
1 x |
maxgraft® bonering 4.1
Recommandé pour des implants de diamètres de 4,1 à 4,5 mm
| N° d’art. | Dimension | Contenu |
|---|---|---|
| 33174 | anneau spongieux, ø 7 mm, hauteur 10 mm
|
1 x |
Distribution
With our international network of distribution partners, we are near you in over 100 countries worldwide. In addition to our 360° productportfolio, we offer service, scientific advice and exchange, training and events directly on site from a single source.
Find a distribution partner near you: