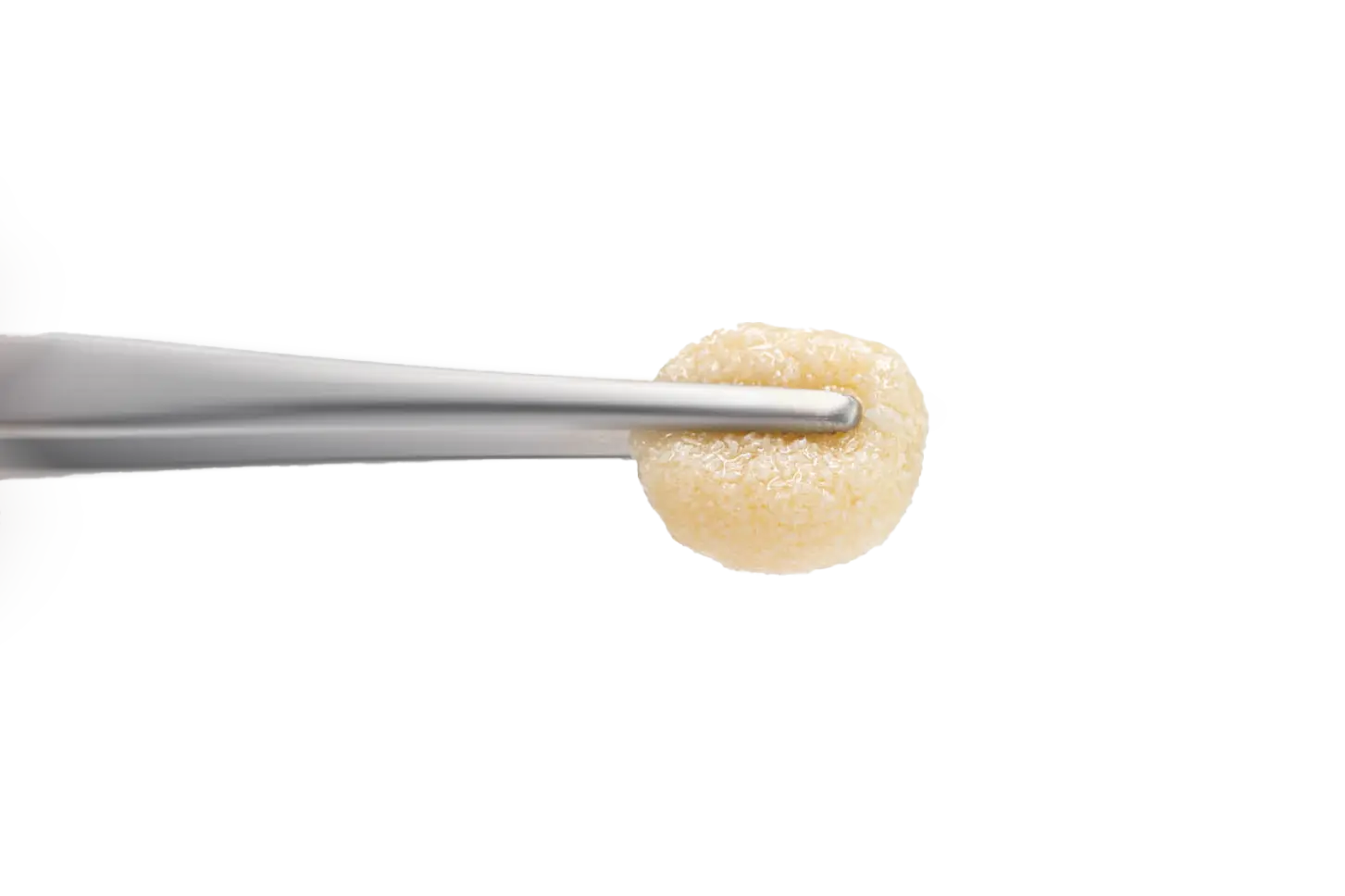
maxgraft® +HyA
Prozessiertes allogenes Knochenersatzmaterial mit Hyaluronat

EInfaches Handling
verbesserte Knochenregeneration
Vorteilhafte Weichgewebeheilung
maxgraft®+HyA erweitert das etablierte maxgraft®-Portfolio durch die Kombination von allogenem Granulat mit Hyaluronat. Aufgrund der außergewöhnlichen flüssigkeitsbindenden Eigenschaften von Hyaluronat ermöglicht maxgraft®+HyA nach der Hydrierung eine optimale Präparation von sticky bone. Die Kombination des hohen biologischen Regenerationspotenzials und dem vollständigen Umbau von maxgraft®, sowie den einzigartigen Vorteilen des Hyaluronats, verbessert die klinischen Ergebnisse und unterstützt die Heilung von Weichgewebe. 1-3
Klinische Vielseitigkeit mit vier Optionen
Rein spongiöses maxgraft®+HyA (kleines und großes Granulat) bietet ein hochporöses Gerüst, das eine optimale Revaskularisierung und Zellversorgung unterstützt, wodurch eine schnelle Regeneration von vitalem Knochengewebe ermöglicht wird.4 Die kortiko-spongiöse Variante (kleines Granulat), die aus ca. 70% kortikalen und 30% spongiösen Knochenpartikeln besteht, bietet eine verbesserte Volumenstabilität. Dies macht es besonders vorteilhaft für die gesteuerte Knochenregeneration in der ästhetischen Zone, wo ein vorhersehbarer Volumenerhalt und die Integration von Weichgewebe wichtig sind. Die extra kleine kortiko-spongiöse Variante (XS-Granulat) bildet nach der Hydrierung eine pastenartige Konsistenz, die einfache Applikation mit einer herkömmlichen Luer-Tip-Spritze ermöglicht – ideal für die Augmentation kleiner oder schmaler Defekte.
IMPLANTOLOGIE, PARODONTOLOGIE, ORAL- UND MUND-, KIEFER-, GESICHTSCHIRURGIE
- Intraossäre parodontale Defekte
- Regeneration von Extraktionsalveolen (Socket Preservation)
- Regeneration von fehlendem Knochengewebe um Zahnimplantate
- Regeneration von Lücken um Blockaugmentationen
- Sinusaugmentation
- Horizontale und vertikale Kieferkammaugmentationen
Anwendung
maxgraft®+HyA muss vor der Anwendung hydriert werden (ca. 0,8 ml Kochsalzlösung oder Patientenblut pro 1 ml maxgraft®+HyA), was unkompliziert in dem mitgelieferten Gefäß erfolgen kann. Detaillierte Empfehlungen zu den Hydrierungsvolumina unter Berücksichtigung der Zusammensetzung der verschiedenen Varianten finden Sie in der Gebrauchsanweisung.
Hydrierung
Geben Sie die Flüssigkeit für die Hydrierung tropfenweise hinzu und passen Sie die Konsistenz nach Belieben an. Verwenden Sie eine 1-ml-Spritze, um das Volumen der Flüssigkeit für die Hydrierung abzumessen und einheitliche Ergebnisse zu erzielen. Aufgrund der Fähigkeit von maxgraft®+HyA, schnell Blut aus der Defektstelle aufzunehmen, wird empfohlen, bei der Hydrierung des Materials eine relativ trockene Konsistenz anzustreben.
Kombination mit autologem Knochen
Wenn Sie mit autologem Knochen arbeiten, sollten die Knochenspäne vor der Hydrierung zu maxgraft®+HyA hinzugefügt werden. Die benötigte Flüssigkeitsmenge kann vom Hydrierungsprotokoll abweichen und sollte durch vorsichtige tropfenweise Zugabe der Flüssigkeit ermittelt werden.
XS-Variante
Die extra kleine (XS) Variante (Granulat < 0,25 mm) bildet nach der Hydrierung eine pastenartige Konsistenz und kann dann in eine herkömmliche 5-6 ml Luer-Tip-Spritze zur präzisen Applikation in kleinen Defekten umgefüllt werden. Zusätzlich kann eine Nadel* angebracht werden, um die Platzierung des Knochenersatzmaterials in schmalen Defekten, wie z.B. in Lücken um Implantaten oder parodontalen Defekten, zu erleichtern.
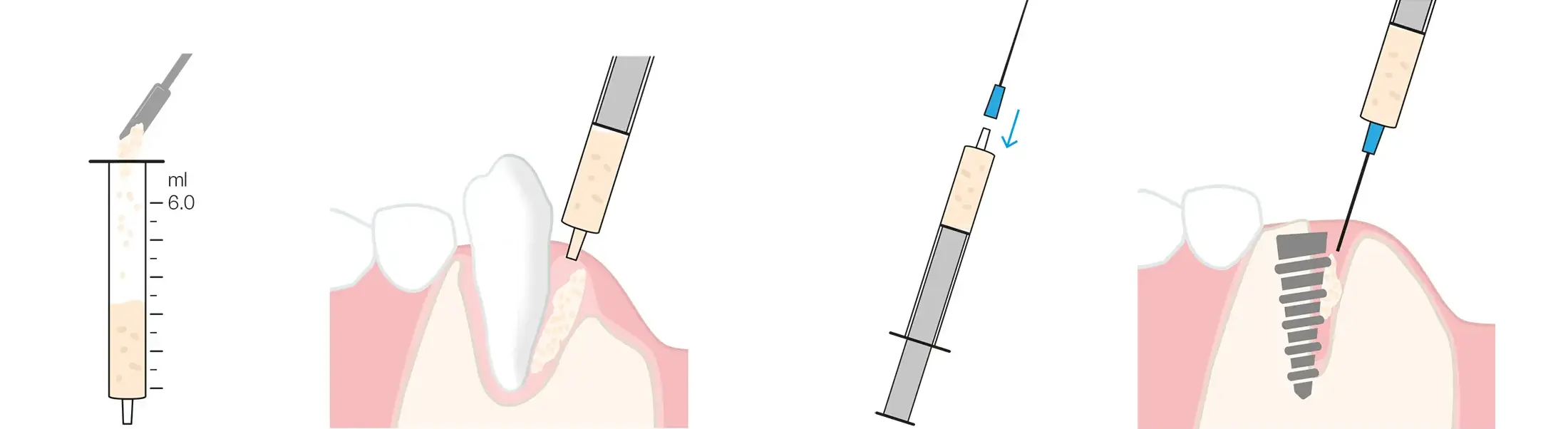
* Empfohlene Größe: 14G/ø 2,1 mm. Beispiel für eine geeignete Nadel: transcodent™ Dental Needle 2.1 x 39 mm. Art. Nr. 162062
Fixierung
Die gründliche Fixierung mit einer Barrieremembran unterstützt die Stabilisierung des Knochenaufbaumaterials an der Applikationsstelle. Um das Einwachsen von Weichgewebe zu verhindern und eine ungestörte Heilung zu ermöglichen, sollte der Augmentationsbereich also mit einer Barrieremembran nach den Prinzipien der GBR abgedeckt werden.
Verwendung des Botiss-Grafters
Der Botiss-Grafter ermöglicht eine mühelose Haydrierung und effiziente Applikation von maxgraft®+HyA (kleine und große Varianten). Außerdem können auch Mischungen aus maxgraft®+HyA und autologem Knochen oder cerabone® in der Applikation mit dem Grafter genutzt werden. Zur homogenen Verteilung sollten die Materialien im gewünschten Verhältnis gemischt werden, bevor sie in den Grafter gefüllt werden. Und so geht es.
- Verbessertes Handling 1,2
- Präzise Applikation an der Defektstelle 2
- Verbesserte Knochenregeneration 3
- Vorteilhafte Weichgewebeheilung1
- Knochenstruktur und Kollagenanteil des menschlichen Knochens bleibt im Knochenersatzmaterial erhalten 5,6
- Kontrollierter Umbau in patienteneigenen Knochen 4,7
Sie sehen gerade einen Platzhalterinhalt von Vimeo. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenProduktspezifikationen
maxgraft® +HyA spongiöses Granulat
| Art.-Nr. | maxgraft® Partikelgröße | Inhalt |
|---|---|---|
| 38005S | 0,25 – 1,0 mm | 1 x 0,5 ml |
| 38010S | 0,25 – 1,0 mm | 1 x 1 ml |
| 38020S | 0,25 – 1,0 mm | 1 x 2 ml |
| 38005L | 1,0 – 2,0 mm | 1 x 0,5 ml |
| 38010L | 1,0 – 2,0 mm | 1 x 1 ml |
| 38020L | 1,0 – 2,0 mm | 1 x 2 ml |
maxgraft® +HyA kortiko-spongiöses Granulat
| Art.-Nr. | maxgraft® Partikelgröße | Inhalt |
|---|---|---|
| 34005XS | < 0,25 mm | 1 x 0,5 ml |
| 34010XS | < 0,25 mm | 1 x 1 ml |
| 34005S | 0,25 – 1,0 mm | 1 x 0,5 ml |
| 34010S | 0,25 – 1,0 mm | 1 x 1 ml |
| 34020S | 0,25 – 1,0 mm | 1 x 2 ml |
Distribution
With our international network of distribution partners, we are near you in over 100 countries worldwide. In addition to our 360° productportfolio, we offer service, scientific advice and exchange, training and events directly on site from a single source.
Find a distribution partner near you:
Verwandte Produkte

cerabone® plus
Natürliches bovines Knochenersatzmaterial mit Hyaluronat
Vereint das bewährte bovine Knochenersatzmaterial cerabone® mit den bekannten Eigenschaften der Hyaluronsäure.
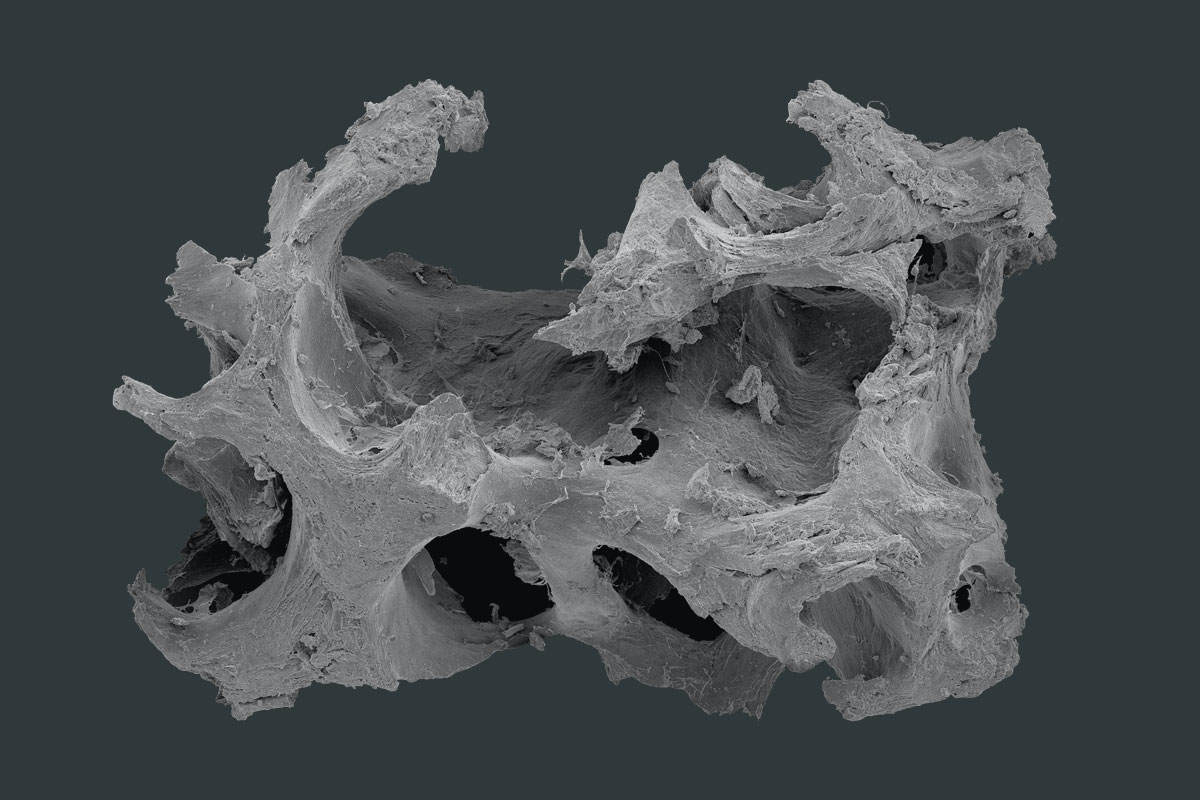
maxgraft® granules
PROZESSIERTES HUMANES ALLOGRAFT
Allogenes Knochenersatzmaterial aus humanem Spenderknochen, das von der Cells+Tissuebank Austria im Allotec®-Verfahren aufbereitet wird